سرطان خون ( لوسمی )
خون از مایع لزجی به نام پلاسما و یاخته های شناور آن که توسط مغز استخوان تولید
می شود تشکیل شده است
مغز استخوان ماده ای نرم و اسفنجی شکل است که داخل استخوانها یافت می شود. این ماده حاوی یاخته هایی است که یاخته های مادر یا سلول پایه (Stem cell) نامیده می شود و وظیفه آنها تولید یاخته های خونی است.
سه نوع یاخته خونی وجود دارد :
گویچه های سفید خون (گلبولهای سفید) که مسئول دفاع بدن در مقابل عوامل خارجی هستندگویچههای قرمز خون (گلبولهای قرمز خون) که اکسیژن را به بافتها حمل کرده و فرآورده های زائد را از اندامها و بافتها جمع آوری می کنندپلاکتها که وظیفه انعقاد خون و جلوگیری از خونریزی را بر عهده دارند
سرطان خون (لوسمی) نوعی بیماری پیشرونده و بدخیم اعضای خون ساز بدن است که با تکثیر و تکامل ناقص گویچههای سفید خون و پیش سازهای آن در خون و مغز استخوان ایجاد می شود.
لوسمی یا لوکمی leukemia ریشه در زبان لاتین به معنای “خون سفید” دارد و فرآیند تکثیر، خونسازی و ایمنی طبیعی بدن را مختل می کند. اجتماع این یاخته های سرطانی در خارج از مغز استخوان، موجب تشکیل توده هایی در اندامهای حیاتی بدن نظیر مغز و یا بزرگ شدن غده های لنفاوی، طحال، کبد و ناهنجاری عملکرد اندامهای حیاتی بدن می شوند.
لوسمی شایع ترین سرطان اطفال در جهان است.
لوسمی براساس طیف، شدت و سرعت پیشرفت روند بیماری به دو دسته حاد (acute) و مزمن (chronic) تعریف می شود.
۱- لوسمی حاد، رشد سریع همراه با تعداد زیادی گویچه های سفید نارس است و مدت فاصله زمانی بین شروع بیماری و گسترش دامنه آن بسیار کوتاه است.
۲- لوسمی مزمن، رشد آهسته همراه با تعداد بیشتری یاخته های سرطانی بالغ تر است و مدت زمان طولانی تا بروز علائم بالینی آن دارد.
لوسمی نیز با توجه به نوع یاخته موجود در بافت مغز استخوان که دچار تراریختی و سرطان شده است تعریف می شود و اشکال مختلفی از این نوع سرطان وجود دارد که هر کدام نشانه ها و عوارض خاص خود را دارند.
لوسمی بر اساس نوع گویچه سفید خون که دچار تراریختگی و سرطان شده به دو دسته تقسیم می شود:
i) لنفوئیدی (lymphocytic) یا لنفوبلاستی ( lymphoblastic)
ii) میلوئیدی ( myelogenous )
با توجه به طبقه بندی فوق، شایع ترین اشکال لوسمی بر اساس سرعت پیشرفت روند بیماری و نوع گویچه سفید خون که دچار تراریختگی و سرطان شده به چهار گروه تقسیم می شود که عبارتند از:
۱- لوسمی لنفوئیدی یا لنفو بلاستی حاد: لوسمی لنفو بلاستی حاد بیماریی است که در آن تعداد بسیار زیادی از گویچه های سفید خون که مسئول دفاع بدن در مقابل عوامل خارجی هستند و “لنفوسیت” نامیده می شوند و هنوز به طور کامل تکامل نیافته اند دچار اختلال شده و بطور فزاینده ای در خون محیطی (blood peripheral) و مغز استخوان یافت می شوند. علاوه بر این، تجمع این یاخته ها در بافتهای لنفاوی باعث بزرگ شدن این اندامها می شود. ازدیاد لنفوسیتها نیر منجر به کاهش تعداد سایر یاختههای خونی مانند گویچههای قرمز و پلاکت ها شده و این عدم تعادل یاختههای خونی منجر به کم خونی، خونریزی و عدم انعقاد خون می شود. مدت فاصله زمانی بین شروع بیماری و گسترش دامنه آن بسیار سریع و کوتاه است. لوسمی لنفوبلاستی حاد، شایع ترین نوع لوسمی در اطفال است که اغلب در کودکان بین سنین ۲ تا ۶ سال تظاهر می کند. گروه سنی دیگری که در مقابل این بیماری بیش از بقیه آسیب پذیر هستند، افراد بالای ۷۵ سال را تشکیل می دهند.
۲- لوسمی میلوئیدی حاد: تراریختگی یاخته های “میلوئید” گویچه های سفید خون است که فرآیند تکثیر و خونسازی و ایمنی طبیعی بدن را مختل می کند. این نوع سرطان دارای چندین زیرگونه و میانگین سن ابتلا به آن ۶۴ سال است. این نوع لوسمی در مقایسه با لوسمی لنفوسیتی حاد کمتر در کودکان دیده می شود اما کودکان مبتلا به سندرم دان (Down Syndrome) در سه سال ابتدایی زندگی استعداد بیشتری برای ابتلا به آن دارند.
۳- لوسمی لنفوئیدی مزمن: شایع ترین نوع لوسمی بزرگسالان است. طیف رشد و پیشرفت این نوع لوسمی بسیار کند و آهسته است و اغلب در افراد سالمند تظاهر می کند. میانگین سن بروز لوسمی لنفوئیدی مزمن ۶۰ سال است و ابتلا به آن در سنین پایین تر از ۳۰ سال بسیار غیر طبیعی و در کودکان بسیار نادر است. این نوع لوسمی در مردان بالای ۵۰ سال شایع تر است و اغلب به طور تصادفی و هنگام معاینات و آزمایش معمولی خون که افراد برای تشخیص بیماری های دیگر انجام می دهند، تشخیص داده می شود.
۴- لوسمی میلوئیدی مزمن: این نوع لوسمی یک بیماری اکتسابی ناشی از یک نوع ناهنجاری در کروموزوم ۲۲ یاخته های مغز استخوان است. لوسمی میلوئیدی مزمن در مردان بین سنین ۴۰ تا ۶۰ سال شایع تر است و افرادی که تحت تشعشعات یونیزه و یا تماس با بنزین و مشتقات آن قرار داشته اند، بیشتر در معرض خطر ابتلا به آن هستند.
سلولهای بنیادی
سلول بنیادی یا بُنیاخته یاختههای اولیهای هستند که توانایی تبدیل و تمایز به انواع مختلف سلولهای دیگر را دارند و از آنها میتوان در تولید سلولها و نهایتاً بافتهای مختلف دیگر استفاده کرد.
منابع اصلی سلولهای بنیادی شامل: مغز استخوان، بند ناف و جفت میباشد. امروزه استفاده از این سلولها جهت ترمیم بافتهای آسیب دیده در حال گسترش است.
جالب این که سلولهای بنیادی پرتوان (چند پتانسیلی) هستند یعنی قابلیت تبدیل به بافتهای مختلف را دارند اعم از بافت عصبی، بافت ماهیچهای، بافت پوششی و غیره. که این توانایی محور اصلی توجه به سلولهای بنیادی است.
مزیت اصلی بنیاختههای بند ناف این است که بسیار اولیه بوده و توان تمایز بالایی دارند. همچنین سلولهای بنیادی گرفته شده از مغز استخوان (BMSCs) توان تمایز بالایی دارند.
ویژگیهای سلولهای بنیادی
1)توان نوسازی: سلولهای بنیادی سلولهای نامتمایزی هستند که توانایی تکثیر نامحدود خود را دارند و در حالت نامتمایز باقی بمانند.
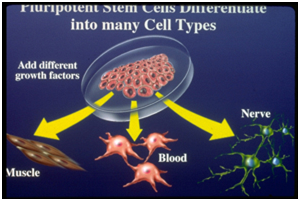
2)پرتوانی: سلولهای بنیادی قادر به ایجاد هر نوع سلولی در بدن هستند. آنها میتوانند تحت تأثیر فاکتورهای رشد مختلف در محیط کشت به سلولهایی با عملکردهای اختصاصی مانند سلولهای ماهیچهای قلب یا سلولهای تولیدکننده انسولین در پانکراس و... تبدیل شوند.
انواع سلولهای بنیادی
1)سلولهای بنیادی جنینی: این سلولها از جنینهای ۴ یا پنج روزه که از تخمهای آزمایشگاهی بارور میشوند به دست میآیند و در محیط آزمایشگاهی در محیط کشتهای اختصاصی رشد داده میشوند.
2)سلولهای بنیادی بالغین: سلولهای بنیادی بالغین، سلولهای نامتمایزی هستند که در بین سلولهای تمایز یافته بافتها و اندامهای بدن یافت میشوند و توانایی نوسازی و تمایز به انواع سلولهای اختصاصی اصلی بافت یا اندام را دارند. نقشهای اولیه این سلولها در یک ارگان زنده شامل حمایت کردن و تعمیر بافتهایی است که از آنها به دست میآیند.
3)سلول های بنیادی خون بند ناف: خون بند ناف خونی است که پس از تولد در بند ناف و جفت باقی می ماند و همراه آن به دور انداخته می شود. این خون علاوه بر سلول های خونی منبعی غنی از سلول های بنیادی خون ساز است. سلول های بنیادی خون ساز می توانند با جایگزین شدن در مغز استخوان فرد بیمار، تامین کننده سلول های خونی جدید باشند. ویژگی مهم سلول های خونی بند ناف عدم تکامل سلول های خونی از جمله لنفوسیت های آن است که در نتیجه احتمال رد پیوندهای انجام شده با این سلول ها در مقایسه با پیوندهای مغز استخوان بسیار کمتر خواهد بود. مطالعات آزمایشگاهی نشان داده اند که سلول های بنیادی خونساز توانایی تمایز به سایر سلول ها را نیز دارند که می توانند افق جدیدی را برای درمان بیماری ها در آینده ای نه چندان دور ترسیم کنند.
کشت سلولهای بنیادی
جنین ۳ تا ۵ روزه را بلاستوسیست مینامند. یک بلاستوسیست تودهای مشکل از ۱۰۰ سلول و یا بیشتر است. سلولهای بنیادی سلولهای درونی بلاستوسیست هستند که در نهایت به هر سلول، بافت و اندام درون بدن تبدیل میشوند.
رشد سلولهای بنیادی در محیط آزمایشگاه را اصطلاحا کشت سلولی مینامند.در واقع جدا کردن سلولهای بنیادی جنینی از طریق انتقال سطح داخلی بلاستوسیست به یک ظرف کشت آزمایشگاهی پلاستیکی که شامل یک بستر تغذیهای به نام محیط کشت میباشد انجام میگیرد. تقسیم و ازدیاد سلولها بر روی سطح این ظرف انجام میگیرد. سطح داخلی این ظرف معمولاً به وسیله سلولهای پوست جنین موش پوشیده شدهاست. این سلولها قادر به تقسیم شدن نیستند. به این لایه پوشاننده سلولی در اصطلاح لایه تغذیهای (feeder layer) گفته میشود. دلیل استفاده از این سلولها فراهم آوردن یک سطح طبیعی به منظور چسپیدن سلولهای بنیادی به آن و عدم جداشدنشان است. در ضمن سلولهای این لایه مواد مغذی را به داخل محیط کشت رها میکنند.
پس از چند روز سلولهای کشت داده شده شروع به رشد و تقسیم شدن در این محیط میکنند. هنگامی که این عمل انجام گرفت سلولهای کشت داده شده که زیاد شدهاند را از این محیط برداشته و به محیطهای تازه کشت منتقل میدهند. پروسه کشت مجدد سلولها بارها و بارها برای چندین مرتبه و به مدت چندین ماه تکرار میشود. بعد از ۶ ماه یا بیشتر ۳۰ سلول اولیه تبدیل به هزاران میلیون سلول بنیادی جنینی میشوند. سلولهایی را که در این دوره ۶ ماه و در این محیط کشت مخصوص تقسیم شده و در عین حال تماییز نیابند را پرتوان (pluripoten) مینامند.
کاربردهای سلولهای بنیادی
- بیماران قلبی:
توصیه میشود برای افرادی که در مراحل وخیم بیماری قلبی بوده و در انتظار دریافت قلب پیوندی بهسر میبرند، در کنار تجویز داروهای سرکوبکننده سیستم ایمنی، از روش پیوند سلولهای بندناف بهعنوان یک روش کمکی استفاده کرد.
- بیماران کبدی:
در حال حاضر اگر بیماری دچار سرطان کبد باشد، جراح مجبور است برای جلوگیری از انتشار سرطان (متاستاز) به بخشهای دیگر بدن، بخش سرطانی کبد را نابود کند. برای این منظور معمولاً طی دو عمل جراحی همزمان، خون ناحیه سرطانی کبد را قطع میکنند تا بافت آن را بازسازی کنند. شبیه سازی انسان مساله دیگر نیز مورد اختلاف شبیه سازی انسان است.
- درمان ریزش مو
- درمتن قرنیه
خصوصیات سلول های بنیادی
1) سلول های تخصص نیافته می باشند که به مدت طولانی از طریق تقسیم سلولی خود را نوسازی می کنند .
بر خلاف سلول های عصبی که معمولاً خودشان را بازسازی نمی کنند این سلول ها ممکن است چندین بار خود را بازسازی کنند، که این پدیده تکثیر کردن نامیده می شود .
2).تحت شرایط فیزیولوژیکی یا آزمایشی، می توان آن ها را تحریک کرد تا به سلول هایی با عمل کردهایی ویژه نظیر سلولهای تپنده ماهیچه ی قلب به سلول های انسولین ساز لوزالمعده تبدیل شوند
تفاوت تک لپه ای ها و دو لپه ای ها
نهان دانگان به دو گروه تک لپه ای و دو لپه ای تقسیم می شوند.
نهان دانگان تک لپه:
ـ گیاهک دانه تنها یک لپه دارد.
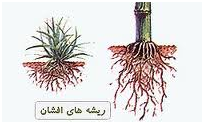
ـ غالبا ریشه افشان و ساقه زیر زمینی یا پیاز دارند.
ـ ساقه هوایی آنها اغلب فاقد انشعاب است، مگر در بخش تشکیل گل، که ممکن است انشعاباتی داشته باشد.
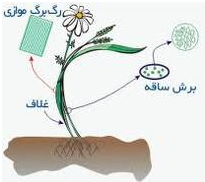
ـ اغلب برگهای گیاهان تک لپه ای دمبرگ ندارند، در عوض به وسیله نیام، دور ساقه را احاطه می کنند .پهنک برگ تقریبا در اغلب تک لپه ایها کشیده و رگبرگها موازی هستند و رگبرگهای موازی به وسیله رگبرگهای مویین به هم مربوط می شوند.
ـ تعداد قطعات گل اغلب سه یا مضربی از این عدد است.
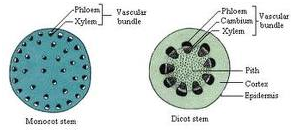
ـ دستجات آوندی بصورت پراکنده هستند .
مثالها:
گندم ، برنج، ذرت و خرما....وانیل و زعفران
زنبق، گل اختر، لاله، سنبل و ثعلب
نهان دانگان دو لپه:
ـ گیاهک دانه دارای دو لپه است.
ـ اغلب آنها ریشه راست دارند.
ـ ساقه هوایی آنها اغلب منشعب است.
ـ برگها دارای گوناگونی فراوان بوده، رگبرگهای آنها اغلب منشعب و غیر موازی است.
ـ تعداد قطعات گل در آنها ۲ یا ۵ یا مضربی از این اعداد است.
ـ دستجات آوندی در یک حلقه قرار دارند.
مثالها:
به سه گروه بی گلبرگ، جدا گلبرگ و پیوسته گلبرگ تقسیم می شوند.
بی گلبرگ:بید،فندق، بلوط و گردو
جدا گلبرگ:تیره های شب بو، خشخاش، مرکبات، گل سرخ و باقلا
پیوسته گلبرگ:تیره های گل میمون، نعناع، گاو زبان، و سیب زمینی


مرگ مغزی :
در حدود یکصد سال پیش پزشکان متوجه وجود بیمارانی شدند که قلبشان پس از « ایست تنفسی » تا مدت زمانی به ضربان خود ادامه می داد . آنها قادر بودند با وسایل اولیة خود به تنفس این بیمارا ن کمک کنند . از جملة این دانشمندان می توان « هورسلی» را نام برد . « هاروی کوشینگ» در سال ۱۹۰۲ موردی را در باره بیماری گزارش کرد که در اثر ازدیاد فشار داخل جمجمه ، به خاطر غدة مغزی ، دچار ایست تنفسی شده بود ولی قلب او تا ۲۳ ساعت بعد به ضربان خود ادامه داد . « مولارت» در سال ۱۹۵۹ بیماری را که مدتها با تنفس مصنوعی زنده نگهداشته بود کالبد شکافی کرد و متوجه شد که در مغز او مناطق وسیعی از انهدام سلولی و ورم مغزی وجود دارند .
از سالهای ۱۹۶۵ تا ۱۹۷۲ به تدریج معیارهای کنونی مرگ مغزی در دانشگاه هاروارد و انستیتوی ملّی بهداشت آمریکا مشخص شدند ، ولی تا دهة هشتاد محرز نشده بود که چقدر از شبکیة پیچیدة عصبی بایستی از بین رفته باشد تا بتوان عنوان « مرگ مغزی» را به آن اطلاق کرد .هنوز هم مسئله به طور کامل مورد قبول واقع نشده است .
مثلاً پژوهشگرانی هستند که میل دارند بیمارانی را که « وظایف عالی» مغز را از دست داده اند جزءافرادی بیاورند که درحقیقت مرده اند . این بیماران شعور ،عقل ، تکلم …..خود را از دست داده اند و با سلسلة اعصاب نباتی زندگی می کنند . اما این پژوهشگران با مخالفت های شدید اخلاقی و فرهنگی روبرو هستند .
پس باید گفت که در مرگ مغزی « هوشیاری» بیمار تبدیل به اغماء شده و « وظایف عالی» مغز نیز برای همیشه ناپدید شده اند . دراصل ، « سطح هوشیاری» توسط ساختمان مشبک ساقة مغز و « وظایف عالی» مغز توسط نیمکره تعیین می شوند .
مرگ مغزی عبارتست از قطع تمامی فعالیتهای مغزی و ساقه مغزی بطور همزمان. فرد مبتلا به مرگ مغزی در واقع شخصی است که بعلت آسیب گسترده به مغز قادر به ایجاد ارتباط با محیط پیرامونش نبوده ، نمی تواند صحبت کند ، نمی بیند ، به تحریکات دردناک پاسخ نمی دهد. فرد مبتلا به مرگ مغزی قادر به تنفس خودبخودی هم نمی باشد. این فرد علیرغم آنکه ضربان قلب دارد وقتی امواج مغزی وی را ثبت کنیم هیچ موج قابل ثبتی ندارد. ضربان قلب وی به کمک دستگاه تنفس مصنوعی و اقدامات نگهدارنده ادامه می یابد تا اعضای اهدایی جهت پیوند در شرایط مطلوب حفظ شوند
مرگ مغزی عبارتست از قطع غیرقابل برگشت کلیه فعالیت های مغزی کورتیکال – ساب کورتیکال و ساقه مغزی بطور همزمان منطبق با شرایط و مشخصه های بالینی و پاراکلینیک عنوان شده در بندهای مرتبط با رعایت تبصره های ملحوظ آسیب و تخریب غیر قابل جبران به نیمکره ها و ساقة مغز را مرگ مغزی گویند .محو کامل تظاهرات فیزیولوژیک قشر خاکستری و هسته های قاعدة مغز و همچنین ساختمان مشبک و سایر اجزاء ساقة مغز به عنوان مرگ مغزی تلقی می شود .تظاهرات بالینی شخص بیمار ظاهراً خواب بوده ولی در اصل در وضعیّت اغماست و به هیچ وسیله یا تحریک درد آور نمی توان با او تماس دهنی برقرار کرده و یا حتی تظاهرات انفعالی در او مشاهده کرد .روش هائی که معمولاً برای تماس ذهنی با بیمار در حال اغماء مورد استفاده قرار می گیرند عبارتند از : حرف زدن با او ، تکان دادن بدن او و یا فشارآور روی ناخن او وارد کردن .
شرایط تلقی مرگ مغزی سه مورد می باشند :
الف) بیمار در اغمای عمیق باشد شواهدی دال بر مصرف داروهای تضعیف کننده دستگاه عصبی مرکزی وجود نداشته باشد.
شواهدی دال بر هیپوترمی (دمای کمتر از ۳۲ درجه) بعنوان عامل اغما وجود نداشته باشد . اختلالات متابولیک – توکسیک – اندوکرین عامل اغمای بیمار نباشند .
ب) قطع کامل تنفس و عدم وجود تنفس خودبخودی که موجب وابستگی و نیاز قطعی به دستگاه تنفس مصنوعی (ونتیلاتور) گردیده است. در این مورد رد مصرف داروهای شل کننده (عوامل مهار کننده عصبی عضلانی) و سایر داروها بعنوان عامل نارسایی تنفسی ضروری است .
ج) با اقدامات معمول علت اغما حتی الامکان مشخص شده باشد .
بررسی های بالینی لازم عبارتند از:الف) عدم حرکات خودبخودی و عدم پاسخ به شدیدترین تحریکات دردناک(Absent Brain Stem Reflexes)
ب) فقدان بازتابهای ساقه مغز .قطر مردمک ها ثابت بوده و به تحریکات نوری با شدت های متفاوت پاسخی مشاهده نمی شود (occulo vesibular عدم وجود واکنش چشمی – دهلیزی (آزمون کالریک یا -عدم وجود واکنش گاگ -تایید نهایی یافته های بالینی با انجام و اثبات آزمون های پاراکلینیک تکمیلی صورت می پذیرد.
الف) تست آپنه مثبت به شرح مقابل : ۱۰ دقیقه قبل از جدا شدن از دستگاه ونتیلاتور (تنفس مصنوعی) به بیمار اکسیژن ۱۰۰% داده می شود و پس از جدا شدن از دستگاه اکسیژن به میزان ۶ لیتر در دقیقه داده شده و اجازه داده می شود تا (فشار دی اکسید کربن) به حد شصت میلیمتر جیوه برسد. در صورت عدم مشاهده هرگونه فعالیت تنفسی تست آپنه مثبت و مؤید مرگ مغزی می باشد
ب) انجام نوار مغزی در دو نوبت و حداقل به فاصله شش ساعت و هر نوبت بمدت بیست دقیقه. ایزوالکتریک بودن نوار مغزی در دو نوبت مؤید مرگ مغزی می باشد
کلیه یافته های بالینی و آزمون ها باید بمدت ۲۴ ساعت بدون تغییربمانند
پزشکان تعیین کننده مرگ مغزی که تکمیل کننده برگه مخصوص تایید مرگ مغزی می باشند شامل دو پزشک متخصص نورولوژی و یا یک متخصص نورولوژی و یک متخصص جراحی مغزواعصاب می باشد که هرکدام جداگانه بیمار را معاینه و بررسی نموده و برگه مخصوص را تکمیل ممهور و امضاء می نمایند. همچنین برگه مذکور توسط یک پزشک متخصص بیهوشی و پزشک نماینده سازمان پزشکی قانونی کشور ممهور و امضاء می گردد .در مورد کودکان زیر ۵ سال زمان نگهداری بیمار تحت دستگاه تنفس مصنوعی حداقل ۷۲ ساعت می باشد
مرگ مغزی چه تفاوتی با اغما (کوما) دارد؟
اغما کاهش اعمال مغز است. در اغما احتمال برگشت هوشیاری وجود دارد، ولی مرگ مغزی ، فقدان برگشت ناپذیر همه فعالیت های مغز است و شانسی برای بهبود ی بعد از مرگ مغزی وجود ندارد. در حالت اغما شخص ممکن است برای مدت طولانی زنده بماند و زندگی نباتی پیدا کند، ولی در مرگ مغزی ، فرد حتماً بعد از چند ساعت یا نهایتاً چند روز فوت خواهد کرد.
چرا فرد دچار مرگ مغزی هنوز قلبش می تپد؟
قلب به دلیل خودکار بودن در صورت داشتن اکسیژن تا مدتی به کار خود ادامه می دهد، ولی یک دستگاه تنفس مصنوعی باید اکسیژن کافی را برای ادامه ضربان قلب فراهم کند. قلب بدون این کمک های مصنوعی از حرکت خواهد ایستاد. حتی با وجود همه این تجهیزات نیز قلب را تا مدت زیادی نمی توان زنده نگه داشت. این مدت از چند ساعت تا چند روز ممکن است طول بکشد.
مرگ مغزی چه تأثیری براعضای دیگر بدن دارد؟
مرگ مغزی یعنی نرسیدن اکسیژن یا جریان خون به مغز، ولی اعضای دیگر بدن مانند قلب، کلیه ها یا کبد تا مدتی زنده و قابل پیوند هستند. این ارگانها، درصورت اقدام به موقع، می تواننددر بدن شخص دیگری به وسیله پیوند اعضا استفاده شوند. با این حال، تخریب اعضای بدن به فاصله کمی پس از مرگ مغزی شروع می شود. به همین علت است که فرایند پیوند اعضا بایدهرچه زودتر انجام شود.
تشخیص بیماری آلزایمر
باانجام همزمان تصویربرداری مغزی و نمونه گیری از مایع نخاعی می توان آلزایمر را خیلی زودتر از ظاهر شدن علائم بیماری تشخیص داد
دانشمندان انگلیسی معتقدند با بررسی میزان چروکیدگی مغز و حجم مایع مغزی نخاع می توان آلزایمر را سال ها قبل از بروز علائم بالینی آن تشخیص داد و با درمان های مناسب، از زوال عقل جلوگیری کرد.
پژوهشگران انگلیسی معتقدند با انجام همزمان تصویربرداری مغزی و نمونه گیری از مایع نخاعی (Lumber Puncture) می توان علائم زوال عقل یا آلزایمر را خیلی زودتر از ظاهر شدن این بیماری تشخیص داد . با استفاده از این روش، پزشکان خواهند توانست بیماری را به طور کامل متوقف کرده یا روند پیشرفت آن را آهسته کنند.درحال حاضر تنها در انگلیس بیش از ۸۰۰هزار نفر مبتلا به آلزایمر زندگی می کنند. از این رو پژوهشگران به دنبال راهی برای درمان یا کند کردن روند پیشرفت بیماری هستند اگرچه داروها و اسکن های زیادی نامزد استفاده در درمان و یا کنترل آلزایمر هستند، اما به علت تشخیص بیماری در مراحل پیشرفته، پزشکان قادر به بررسی عملکرد داروها نیستند.
دکتر جاناتان اسکات و همکارانش از مرکز تحقیقات نورولوژی دانشگاه لندن، بر این باورند که می توان علائم آلزایمر را سال ها قبل از بروز علائم بالینی آن تشخیص داد این پژوهشگران دو فاکتور مهم را در تحقیقات خود مورد مطالعه قرار داده اند؛ یکی میزان چروکیدگی مغز و کاهش پروتئین آمیلوئید و دیگری، بررسی CSF است که مایع مغز نخاع را در برمی گیرد آنها معتقدند که در آلزایمر، حجم مغز کم شده و تولید آمیلوئید در مغز از حالت نرمال خود خارج می شود که در نتیجه به کاهش میزان این ماده در مایع نخاع منجر می شود گروه تحقیقاتی برای تایید ایده خود، ۱۰۵ داوطلب سالم را بررسی کردند و با نمونه گیری از مایع نخاعی، میزان آمیلوئید موجود در CSF را بررسی کردند علاوه بر آن، میزان چروکیدگی مغز این افراد نیز با استفاده از ام.آر.ای مشخص شد.
نتایج تحقیقات نشان داد افرادی که سطح آمیلوئید آنها ۳۸ درصد کاهش یافته، دو برابر سریع تر از سایر افراد دچار چروکیدگی مغز می شوند و احتمال دارا بودن ژن APOE۴ و سطح بالای پروتئین های موثر در آلزایمر در این افراد ۵ برابر سایرین است.